Inleiding
In Nederland worden jaarlijks ongeveer 4000 patiënten behandeld met pemetrexed.1 Pemetrexed is geregistreerd voor de behandeling van maligne pleuraal mesothelioom (MPM) en niet-kleincellig longcarcinoom (NSCLC).2 Als er bij de behandeling met pemetrexed geen dexamethason gegeven wordt krijgen 70-90 procent van de patiënten huidreacties die bij 30-40 procent ernstig verlopen (graad III/IV).3,4 Huidreacties ten gevolge van pemetrexed kunnen zich manifesteren als pruritus, vasculitis, oedeem en ernstige reacties die lijken op toxische epidermale necrolyse.5 Om deze huidreacties te voorkomen dient volgens de summary of product characteristics (SmPC) dexamethason ter profylaxe te worden toegediend in een orale dosering van 4 mg tweemaal daags gedurende drie dagen (de dag voor, de dag van en de dag na de toediening van pemetrexed), wat resulteert in een totale cumulatieve dosis van 24 mg.2 Het toevoegen van dexamethason ter profylaxe reduceerde het aantal allgrade huidreacties tot slechts 14 procent en het aantal graad III/ IV huidreacties tot 0,8 procent.6 De effectiviteit van dexamethason tegen huidreacties is daarmee aangetoond, maar de optimale dosering en toedieningsroute is onderwerp van discussie.7-9 De dosering van dexamethason die in de SmPC aanbevolen wordt is gebaseerd op fase I1studies naar behandeling met pemetrexed, maar een onderbouwing voor deze hoge dosering ontbreekt.10 Dexamethason kan gepaard gaan met ernstige dosisgerelateerde bijwerkingen zoals hyperglykemie, immuunsuppressie en stemmings en slaapstoornissen, wat een negatieve invloed heeft op de kwaliteit van leven.11,12 Dit roept de vraag op of de huidige dosering dexamethason verlaagd kan worden zonder dat dit leidt tot een toename van huidreacties ten gevolge van pemetrexed.
Literatuuroverzicht effectiviteit van lagere doseringen dexamethason
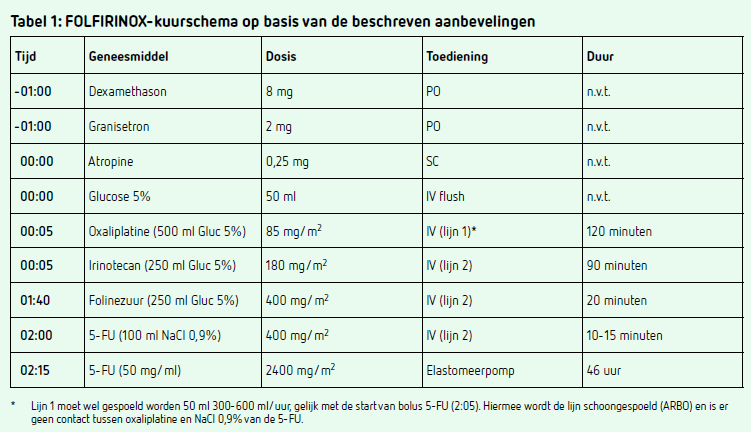
In verschillende studies is onderzoek gedaan naar de optimale dosering dexamethason ter profylaxe van huidreacties ten gevolge van pemetrexed (Tabel 1). Clark et al. (2019) onderzochten in een retrospectieve cohortanalyse (n = 85) met NSCLC- en MPM-patiënten het risico op huidreacties bij pemetrexedgebruik bij een verlaagde dosering dexamethason. Zowel de interventiegroep als de controlegroep kreeg voorafgaand aan de start van pemetrexedtoediening een intraveneuze (IV) dexamethason toediening van 10 mg. De controlegroep kreeg daarnaast ook dexamethason oraal 4 mg tweemaal daags op de dag voor, de dag van en de dag na pemetrexedtoediening. Er werd geen statistisch significant verschil gevonden in de incidentie van huidreacties (allgrade) tussen de interventiegroep en controlegroep (13,8 procent vs. 25,0 procent, p = 0,384). Ook voor graad III/IV huidreacties werd geen statistisch significant verschil gevonden (0 procent vs. 14,3 procent, p = 0,545).13 In een retrospectieve studie (n = 70) van Groleau et al. (2020) leek een eenmalige IV-dosering van dexamethason effectief in het voorkomen van huidreacties ten gevolge van pemetrexedgebruik bij NSCLC-patiënten. Hierin kreeg de interventiegroep een dexamethason toediening van 20 mg IV, terwijl de controlegroep het reguliere driedaagse orale dexamethasonschema kreeg. Er bleek geen statistisch significant verschil in de incidentie van huidreacties (allgrade) tussen respectievelijk de interventiegroep en de controlegroep (23,1 procent vs. 16,1 procent, p = 0,56) en geen van de patiënten kreeg een graad III/IV huidreactie. Hieruit concludeerden de onderzoekers dat deze eenmalige dexamethason toediening van 20 mg IV even effectief is in het voorkomen van huidreacties ten gevolge van pemetrexed als het reguliere dexamethasonschema.7 Sakurada et al. (2022) voerden een singlearm fase IIstudie (n = 24) uit bij pemetrexednaïeve MPM- of NSCLC-patiënten.
Op de dag van pemetrexedtoediening kregen zij 9,9 mg dexamethason IV (bij pemetrexed i.c.m. carboplatine) of 6,6 mg dexamethason IV (bij pemetrexed zonder carboplatine) toegediend. Daarnaast kregen ze van dag 2 tot en met dag 6 na de pemetrexedtoediening dagelijks nog oraal 2 mg dexamethason. Dit resulteerde in een lagere cumulatieve dexamethasondosering van 19,9 mg of 16,6 mg ten opzichte van een reguliere cumulatieve dosering van 24 mg. Bij 4 van de 24 (16,7 procent) patiënten trad binnen 3 weken een huidreactie (allgrade) op (95%-BI: 4,7 37,4) en geen van de patiënten kreeg een graad III/IV huidreactie. Op basis van deze bevindingen en de incidentie van huidreacties zoals beschreven in de literatuur concludeerden de onderzoekers dat deze lagere dosering dexamethason niet leidde tot een hogere incidentie van huidreacties ten gevolge van pemetrexed.14 Ten slotte onderzochten Elsoueidi et al. (2016) in een kleine retrospectieve studie (n = 14) bij NSCLC-patiënten het effect van een eenmalige dosering van 20 mg dexamethason 30 minuten voorafgaand aan pemetrexedtoediening ter profylaxe van huidreacties. In deze studie kregen 8 patiënten dexamethason oraal en 6 patiënten dexamethason IV, waarna geen van hen een huidreactie kreeg. Op basis van deze resultaten concludeerden de onderzoekers dat een eenmalige dosering van 20 mg dexamethason niet zorgt voor een verhoogd risico op huidreacties bij pemetrexedgebruikers.15

Discussie
Dexamethason kan voor ernstige dosisgerelateerde bijwerkingen zorgen. De initiële dosisselectie van dexamethason is mogelijk niet optimaal gekozen in de registratiestudie en kan wellicht worden verlaagd. Het advies van de commissie Doelmatigheid en Duurzaamheid van de NVMO is daarom om de dosering dexamethason rondom pemetrexed te verlagen.
Op dit moment zijn de resultaten van een beperkt aantal studies beschikbaar naar alternatieve dexamethasondoseringen rondom pemetrexed. In deze studies werd een eenmalige intraveneuze toediening van 10 mg of 20 mg gehanteerd. De laagst beschreven dosering is een eenmalige intraveneuze toediening van 10 mg op de dag van pemetrexedtoediening.13 Ook is er een single-arm trial waarin op de dag van pemetrexedtoediening (dag 0) eenmalig IV 9,9 mg (bij pemetrexed i.c.m. carboplatine) of 6,6 mg (bij pemetrexed zonder carboplatine) wordt gegeven, met daarna op dag 2 t/m 6: oraal 1 d.d. 2 mg.14 Gezien het ontbreken van bewijs voor de hoge dosering dexamethason en de ernstige bijwerkingen die hiermee gepaard kunnen gaan, adviseert de commissie de dosering van dexamethason rondom pemetrexed te verlagen. Orale toediening van dexamethason heeft de voorkeur vanwege de lagere kosten en duurzaamheidsvoordelen ten opzichte van IV dexamethason, zonder verschil in effectiviteit. De commissie heeft een expertgroep, bestaande uit 6 longartsen met aandachtsgebied longkanker, geconsulteerd. Zij konden zich vinden in dit advies. Op basis van bovengenoemde studies en deze expert opinion is de commissie tot het advies gekomen de dosering dexamethason te verlagen naar een eenmalige orale dosis van 8 mg voorafgaand aan de behandeling met pemetrexed mits er geen andere matig tot hoogemetogene oncolytica zoals carboplatine gelijktijdig gegeven worden.
Referentie(s)
- Dutch Hospital Data (DHD). Drug monitor. gmm.dhd.nl [Accessed 20-02-2024].
- Geneesmiddeleninformatiebank. Pemetrexed [SmPC]. https://geneesmiddeleninformatiebank.nl/smpc/h125258_smpc.pdf [Accessed 20-02-2024]
- Rusthoven JJ, Eisenhauer E, Butts C, et al. Multitargeted antifolate LY231514 as firstline chemotherapy for patients with advanced nonsmallcell lung cancer: a phase II study. J Clin Oncol 1999;17(4):1194 9.
- Clarke, S.J., et al. Phase II trial of pemetrexed disodium (ALIMTA, LY231514) in chemotherapy-naive patients with advanced non-small-cell lung cancer. Ann Oncol 2002;13(5):737-41.
- Pierard-Franchimont, C., et al. Revisiting cutaneous adverse reactions to pemetrexed. Oncol Lett 2011;2(5):769-72.
- Hanna, N., et al. Randomized phase III trial of pemetrexed versus docetaxel in patients with nonsmallcell lung cancer previously treated with chemotherapy. J Clin Oncol 2023;41(15):2682-90.
- Groleau, A. and J. Cote. Comparison between two premedication regimens of dexamethasone before a pemetrexed-based chemotherapy: A singlecenter experience study. J Oncol Pharm Pract 2020;26(3):612-8.
- Sakurada, T., et al. Pemetrexedinduced rash may be prevented by supplementary corticosteroids. Biol Pharm Bull 2015;38(11):1752-6..
- de Rouw, N., et al., Mechanisms, management and prevention of pemetrexedrelated toxicity. Drug Saf 2021;44(12):1271-81.
- Rinaldi, D.A., et al. A phase I evaluation of multitargeted antifolate (MTA, LY231514), administered every 21 days, utilizing the modified continual reassessment method for dose escalation. Cancer Chemother Pharmacol, 1999;44(5):372-80.
- Vardy, J., et al., Side effects associated with the use of dexamethasone for prophylaxis of delayed emesis after moderately emetogenic chemotherapy. Br J Cancer 2006;94(7):1011-5.
- Fardet, L., et al., Corticosteroidinduced adverse events in adults: frequency, screening and prevention. Drug Saf 2007;30(10):861-81.
- Clark, S.K. and L.M. Anselmo. Incidence of cutaneous reactions with pemetrexed: Comparison of patients who received three days of oral dexamethasone twice daily to patients who did not. J Oncol Pharm Pract 2019;25(7):1645-50.
- Sakurada, T., et al., Prevention of pemetrexedinduced rash using lowdose corticosteroids: a phase II study. Oncologist, 2022;27(7):e554e560.
- Elsoueidi, R., et al., Single-dose dexamethasone for the prevention of pemetrexed associated cutaneous adverse reactions. J Oncol Pharm Pract 2016;22(2):271-4.