
Voorblad
Indicatieaanvraag/studie: capecitabine ipv 5FU bij concomitante chemoradiatie bij urotheelcelcarcinoom (UCC)
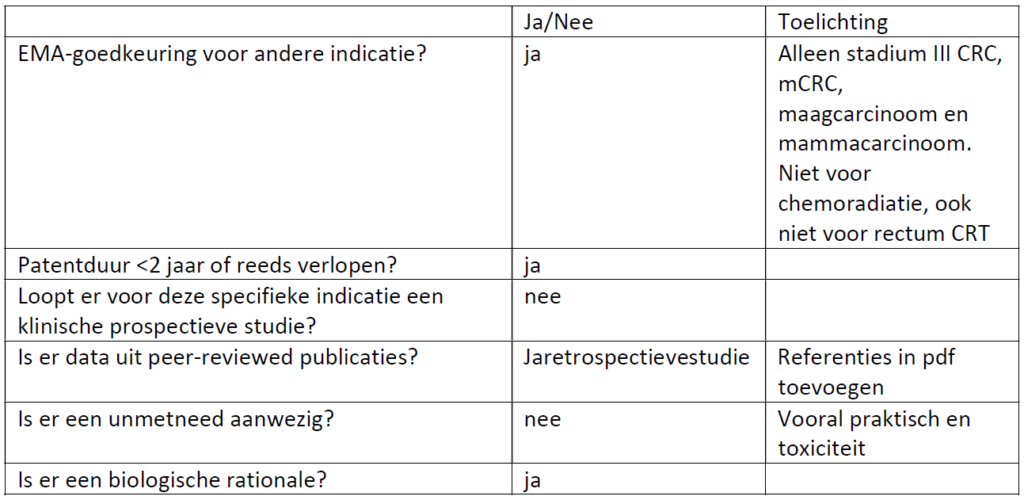
Beoordeling door CieOOM mogelijk: ja
Beoordeling voorleggen aan CieBOM: nee
Denken wij dat er een gerandomiseerde studie mogelijk is: nee - ik denk van niet gezien ingeburgerd
gebruik al van capecitabine en veronderstelde bioequivalentie die maakt dat je een grote sample size
nodig zou hebben om aan te tonen dat 5FU vs capecitabine equivalent is
Waar hoort het thuis:
- Bio equivalentie
Wijze van beoordelen (NRS of niet): Geen NRS
Huidige standaard: 5FU is de standaard of er is geen standaard.
Huidige indicatietekst: NA
Inleiding
In meerdere oncologische indicaties wordt bij behandeling van patiënten met chemoradiatie gebruik gemaakt van 5FU als radiosensitizer. In verband met doseergemak en geen noodzaak tot intraveneuze behandeling wordt regelmatig gekozen voor vervangen van 5FU door capecitabine. Er wordt hierbij uitgegaan van een bioequivalentie van de 2 middelen voor radiosensitizing effectiviteit. Er is off label add-on voor de indicatie chemoradiatie bij rectumcarcinoom (indicatienummer in addon lijst 1381), vulvacarcinoom (1302) en anuscarcinoom (1188).
Hieronder is voor de indicaties capecitabine bij chemoradiatie rectumcarcinoom, anuscarcinoom, vulvacarcinoom en urotheelcelcarcinoom de literatuur samengevat.
Bio equivalentie - basis is de behandeling van rectumcarcinoom
Tumortype, behandellijn (per tumortype aparte lijst)
Rectumcarcinoom
Medicament/middelen
Capecitabine
Huidige standaard en huidige indicatietekst (op farmatec)
Chemoradiatie rectum is standaard met capecitabine; 5FU is oude standaard FarmatecJ rectum CRT 1381
Korte bespreking van de studie(s)
5 retrospective studies, 3 prospective studies, and 2 randomized controlled trials [RCTs]) compared the efficacy of the 5-FU arm (n = 757) to that of the CA arm (n = 719). There was no significant difference in tumor down-staging rate between the 2 regimens (RCTs/prospective studies: odds ratio [OR], 0.88; 95% confidence interval [CI], 0.65-1.20; P = .416; retrospective studies: OR, 0.84; 95% CI, 0.50-1.44; P = .534). There was also no significant difference in pathologic complete response (RCTs/ prospective studies: OR, 0.80; 95% CI, 0.52-1.23; P = .304; retrospective studies: OR, 0.73; 95% CI, 0.48-1.12; P = .149), or survival rates (3-year, 5-year DFS, and 5-year OS rate) between the 2 groups. The CA group had a higher number of patients reporting diarrhea and hand-foot syndrome compared with the 5-FU group. The 5-FU group had a higher number of patients reporting mucositis compared with the CA group.
1 RCT uit 2022 heeft QOL meting meegenomen, n = 63 stage II and III rectal cancer patients, neoCRT with either capecitabine (group 1) or 5-Fu and leucovorin (group 2) concomitant to longcourse radiotherapy. EORTCs QLQ-C30 and CR38 were applied.
32 patients were assigned to group 1 and 31 to group 2. Clinical downstaging occurred in 70.0% of group 1 and 53.3% of group 2 (p = 0.288), and sphincter preservation was 83.3% in group 1 and 80.0% in group 2 (p = 0.111). No significant difference in QOL was detected when comparing the two treatment groups after neoCRT using QLQ-C30. However, the CR38 module detected differences in micturition problems (15.3 points), gastrointestinal problems (15.3 points), defecation problems (11.8 points), and sexual satisfaction (13.3 points) favoring the capecitabine group.
Argumenten voor gelijkwaardigheid
Respons en tumordownstaging vergelijkbaar.
Effectiviteit en toxiciteit
Verschil in toxiciteit: Cape HFS endiarree, 5FU mucositis
Effectiviteit: Tabel 3: DFS, OS, pCR en % downstaging
Bijwerkingen (totaal / gerelateerd aan de behandeling)
Lethaal: % ?
Acuut, ernstig (graad 3-4): %
Staken van de behandeling i.v.m. bijwerkingen: %
Kwaliteit van leven
Kwaliteit van leven analyse: Geen significant verschil in overall QOL, hoewel betere score voor capecitabine tav aantal specifieke items (mictie, gastro-intestinaal en seksueel).
Beperkingen van de studie
Meestretrospectief
Referentie(s)
ClinColorectal Cancer. 2017 Sep;16(3):e123-e139.
Support Care Cancer. 2022 Aug;30(8):6557-6572
Discussie / advies / wanneer herbeoordelen
Uit deze meta analyse uit 2017 en QOL analyse 2022 blijkt dat het aannemelijk is voor rectumcarcinoom dat er een bioequivalentie is van 5FU en capecitabine als radiosensitizer. Eindpunten zijn DFS, OS, pCR en % downstaging. Zie tabel 3 van meta analyse: vergelijkbare
resultaten
Vraag is of dit resultaat als argument kan gebruikt worden voor bioequivalentie bij ook andere
indicaties
Literatuur na 2017 onderstreept bovenstaande conclusie.
Datum besproken vergadering
4 oktober 2022
Tumortype, behandellijn (per tumortype aparte lijst)
anuscarcinoom
Medicament/middelen
Capecitabine vs 5FU
Huidige standaard en huidige indicatietekst (op farmatec)
FarmatecJ anuscarcinoom CRT 1188
Korte bespreking van de studie(s)
De bewijsvoering voor nut van 5FU bij anuscarcinoom chemoradiatie stamt uit de 80-er Jaren 20e eeuw, met alleen cohortstudies van tientallen patienten (ref 1). Nooit gerandomiseerd uitgezocht. Initieel is chemoradiatie ook toegepast als inductiebehandeling conform het concept van rectumcarcinoom, later als definitieve orgaansparende chemoradiatie.
Studie 1: retrospectievevergelijkende serie 107 patientenanuscarcinoom
We retrospectively reviewed the records of 107 consecutive patients with nonmetastatic ASCC treated with definitive chemoradiation from January 2009 to May 2014.
Of 107 patients, 63 were treated with infusional 5-FU (1000 mg/m2/day for 4 days) and mitomycin C (MMC) (10 mg/m2) during weeks 1 and 5, and 44 patients were treated with capecitabine (825 mg/m2 twice daily) Monday through Friday throughout radiation therapy (RT) and MMC (10 mg/m2) during weeks 1 and 5. The incidence of grade 3 to 4 acute toxicity was compared between the 2 groups.
Intensity modulated RT all patients: radiotherapy 56 Gy. In the 5-FU group, 52% experienced grade 3 to 4 neutropenia compared with 20% in the capecitabine group. Treatment breaks resulting from toxicity,primarily related to grade 3þ hematologic toxicity, were necessary for 42% of patients treated with 5-FU versus 16% of those treated with capecitabine The median follow-up time for survivors in the 5-FU group was 49 months versus 22 months in the capecitabine group. The 2-year OS was 87% for the 5-FU group and98% for the capecitabine group The median OSwas not reached in either group The 2-year cumulative incidence of LRR was 6.5% in the 5-FU group and 8.2% in the capecitabine group while the 2-year cumulative incidence of Distant Metastasis was 14.7% in the 5-FU group and 7.6% in the capecitabine group .
Studie 2: retrospectieve vergelijkende serie 105 patienten anuscarcinoom (studie AvL)
One hundred and five patients with squamous cell AC stage T2-4 (T244 cm), N0-1, M0 or T1-4, N2-3, M0, were included in this retrospective study. Forty-seven patients were treated with continuous 5-FU (750mgm_2) on days 1–5 and 29–33, mitomycin C (MMC, 10mg/m2) on day 1, and radiotherapy; 58 patients were treated with capecitabine (825mgm_2 b.i.d. on weekdays), MMC (10mg/m2) on day 1, and radiotherapy. The primary end points of the study were: clinical complete response rate, locoregional control (LRC) and overall survival (OS). Secondary end points were: colostomy-free survival (CFS), toxicity and associations of genetic polymorphisms (GSTT1, GSTM1, GSTP1 and TYMS) with outcome and toxicity.
Results: Clinical complete response was achieved in 41/46 patients (89.1%) with 5-FU and in 52/58 patients (89.7%) with capecitabine. Three-year LRC was 76% and 79% (P=0.690, log-rank test), 3-year OS was 78% and 86% (P=0.364, log-rank test) andCFS was 65% and 79% (P=0.115, log-rank test) for 5-FU and capecitabine, respectively. GSTT1 and TYMS genotypes were associated with severe (grade 3–4) toxicity.
Toxicities gr3-4 5FU vs cape: dermatologic 13 vs 31%; GI 2 vs 3%; haematological 6 vs 6%; GU 4 vs 2 %
Argumenten voor gelijkwaardigheid
Vergelijkbare resultaten in retrospectieve studies contemporain
Beide groepen combinatie met MMC zoals gebruikelijk bij anuscarcinoom
Effectiviteit en toxiciteit
Argumenten:
- Verschil in toxiciteit: Ander profieltoxiciteit
- Effectiviteit: Lijkt vergelijkbaar in beide cohorten
Bijwerkingen (totaal / gerelateerd aan de behandeling)
Lethaal: 0%
Acuut, ernstig (graad 3-4):
- Study 1 hematologic tox 52 à 20% (neutropenie gr 3-4)
- Study 2 Increasedermtox 13 à 31%
Staken van de behandeling i.v.m. bijwerkingen: %
Kwaliteit van leven
Kwaliteit van leven analyse: NB
Beperkingen van de studie
Alleen retrospectieve data
Referentie(s)
- https://pubmed.ncbi.nlm.nih.gov/4830803/
- Annals of Medicine and Surgery, 2020-07-01, Volume 55, Pages 36-46
- Int J RadiatOncolBiol Phys. 2017 Aug 1;98(5):1087-1095. doi:10.1016/j.ijrobp.2017.03.022. Epub 2017 Mar 22
- Br J Cancer. 2014 Oct 28;111(9):1726-33. doi: 10.1038/bjc.2014.467. Epub 2014 Aug 28.
Discussie / advies / wanneer herbeoordelen
Prima (retrospectieve) data waarin series niet-gerandomiseerd vergeleken worden.
Datum besproken vergadering
4-10-2022
Tumortype, behandellijn (per tumortype aparte lijst)
vulvacarcinoom
Medicament/middelen
capecitabine
Huidige standaard en huidige indicatietekst (op farmatec)
Er is geen standaard voor chemoradiatie vulvacarcinoom. Zie ook argumentatie in artikel hieronder: als je CRT geeft zijn er verschillende opties qua chemotherapie maar weinig data tot dit artikel.
FarmatecJ vulvacarcinoom CRT 1302
Korte bespreking van de studie(s)
Fase 2 multicenter studie NL
52 patients with mainly T2/T3 disease were treated. Full dose radiotherapy (tumor dose of 64.8Gy) was delivered in 92% and full dose capecitabine in 69% of patients. Most prevalent acute ≥ grade 3 toxicities were regarding skin/mucosa and pain (54% and 37%). Late ≥grade 3 toxicity was reported for skin/mucosa (10%), fibrosis (4%), GI incontinence (4%) and stress fracture or osteoradionecrosis (4%). Twelve weeks after treatment, local clinical complete response (cCR) and regional control (RC) rates were 62% and 75%, respectively. After 2 years, local cCR persisted in 22 patients (42%) and RC was 58%. Thirty patients (58%) had no evidence of disease at end of follow-up (median 35 months). In 9 patients (17%) extensive surgery with stoma formation was needed. Progression free survival was 58%, 51% and 45% and overall survival was 76%, 66%, 52% at 1,2, and 5 years.
Argumenten voor gelijkwaardigheid
Geen vergelijkende studie, alleen capecitabine
Effectiviteit en toxiciteit
Argumenten:
- Verschil in toxiciteit: Geen vergelijkende studie(s)
Bijwerkingen (totaal / gerelateerd aan de behandeling)
Lethaal: %
Acuut, ernstig (graad 3-4): %
Staken van de behandeling i.v.m. bijwerkingen: %
Kwaliteit van leven
Kwaliteit van leven analyse
Beperkingen van de studie
Enkele behandelarm
Referentie(s)
Gynecologic Oncology, 2021-10-01, Volume 163, Issue 1, Pages 117-124
Discussie / advies / wanneer herbeoordelen
Datum besproken vergadering
Tumortype, behandellijn (per tumortype aparte lijst)
urotheelcelcarcinoom
Medicament/middelen
Capecitabine vs 5FU
Huidige standaard en huidige indicatietekst (op farmatec)
Geen indicatietekst voor capecitabine voor UCC
Korte bespreking van de studie(s)
Achtergrond
Registratiestudie voor chemoradiatie UCC: NEJM 2012 (ref 1); radiotherapie vs chemoradiatie.
55 Gy in 20 fractions over a 4-week period or 64 Gy in 32 fractions over a 6.5-week period in all patients. Fluorouracil was administered as a continuous infusion (500 mg per square meter of body-surface area per day) during fractions 1 to 5 and 16 to 20 of radiotherapy (10 days in total). MMC d1 12 mg/m2 on day 1.
2 jaar locoregionale DFS (LDFS) 67% (95%BI 59-74) bij CRT vs 54% (95% BI 46-62) bij RT. Na mediane FU 69.9 m: HR 0,68 (95% BI 0,48-0,96, p=0,03). 5Y OS 48% (95% BI 40-55) bij CRT en 35% (95% BI 28-43) bij RT, HR 0,82 (95% BI 0,63-1,09, p=0,16).
Huidige studie uit AvL ref 2
Single center retrospectieve studie
CRT (60 Gy in 5 weeks with single-dose MMC 12 mg/m2 and capecitabine orallytwicedaily 825 mg/m2) alle dagen van de bestraling, dus 25 dagen, geen weekenden. We analysed 71 patients cT2-4aN0-2 M0 MIBC (median age 70 years). Twenty-one (30%) patients received neoadjuvant or induction chemotherapy and 14 (20%) patients underwent a pelvic lymph node dissection prior to CRT. All patients received the full dose of planned radiation. Seven (10%) patients experienced acute grade 3–4 toxicities and 2 (3%) patients experienced late grade 3–4 toxicities. Sixty-eight (96%) patients achieved cCR. Eight (11%) patients had a bladder recurrence, of whom 3 (4%) required salvage cystectomy. Two-year LDFS was 79% (95% CI: 68–88) at a median follow-up of 23 (95% CI: 17–28) months.
Oude patienten niet eligible voor intensieve behandeling mediane leeftijd 80 jaar; alleen capecitabine en geen MMC; detroit (ref 3)
Of 14 patients, 3 (20%) required hospitalization for management of toxicities. Seven patients required dose modification, and the therapy was relatively well tolerated. Clinical complete response was seen in 11 of 13 evaluable patients (77%). At a median follow-up of 10.5 months, only 3 of 11 responders had relapsed.
Elderly patients Chicago, alleen capecitabine engeen MMC (ref 4)
Eleven patients (median age, 80 years) with localized disease (n = 7), locally advanced disease (n = 3), or local-only recurrence after cystectomy (n = 1) were treated.
With a median follow-up of 16.6 months, overall survival, progression-free survival, freedom from local failure, and freedom from distant metastasis at 1 year were 82%, 55%, 100%, and 55%, respectively, and at 2 years were 61%, 41%, 80%, and 55%, respectively.
Studie 30 patiënten median 73 jaar egypte (ref 5) alleen cape, geen MMC
After a median follow-up of 16 months, the locoregional control rate was 63%. Overall survival, local failure-free survival, and event-free survival were 100%, 93.3%, 80% and 43.3%, 33.3%, 30% at one and two years respectively.
Argumenten voor gelijkwaardigheid
Geen vergelijking met 5FU chemoradiatie.
Effectiviteit en toxiciteit
Argumenten:
- Verschil in toxiciteit: Onbekend bij UCC
Bijwerkingen (totaal / gerelateerd aan de behandeling)
Lethaal: %
Acuut, ernstig (graad 3-4): %
Staken van de behandeling i.v.m. bijwerkingen: %
Kwaliteit van leven
Kwaliteit van leven analyse: Niet verricht
Beperkingen van de studie
Single center retrospectieve studie
Referentie(s)
- N Engl J Med 2012;366:1477–88. doi:10.1056/NEJMoa1106106.
- Radiotherapy and Oncology, 2020-09-01, Volume 150, Pages 275-280
- Int J RadiatOncolBiol Phys. 2005 Aug 1;62(5):1332-8. doi: 10.1016/j.ijrobp.2005.01.004
- ClinGenitourin Cancer. 2019 Feb;17(1):e12-e18.
- Asian Pac J Cancer Prev. 2022 May 1;23(5):1733-1740. doi: 10.31557/APJCP.2022.23.5.1733.
Discussie / advies / wanneer herbeoordelen
Er is geen vergelijking, maar wel vergelijkbare resultaten van CRT cape/MMCtov de
registratiestudie met CRT 5FU/MMC.
Datum besproken vergadering
4-10-2022
Bespreking resultaten
Voor rectumcarcinoom zijn er overtuigende goede gerandomiseerde prospectieve data die een bioequivalentie van capecitabine aantonen.
Voor anuscarcinoom zijn er retrospectieve vergelijkende data met chemoradiatie MMC/cape versus chemoradiatie MMC/5FU waarbij effectiviteit en toxiciteit vergelijkbaar lijken.
Voor vulvacarcinoom is er één single-arm fase II studie van chemoradiatie met capecitabine met goed gedocumenteerde oncologische uitkomsten en bijwerkingen registratie.
Voor urotheelcelcarcinoom zijn er enkele retrospectieve series van chemoradiatie met MMC/cape en cape monotherapie met vergelijkbare effectiviteits- en toxiciteitsdata als in de grote registratiestudie waarin de meerwaarde van chemoradiatie met 5FU/MMC werd aangetoondtov radiotherapie alleen.
Conclusie en voorstel
Gezien bovenstaande zijn er sterke aanwijzingen dat capecitabine een effectieve, veilige en ook patiënt-vriendelijke vervanger is voor 5FU als radiosensitizer bij in opzet curatieve chemoradiatie in verschillende tumorgroepen (rectum, anus, vulva, urotheelcelcarcinoom). Hierbij is het voorstel om de off-label indicatieteksten voor chemoradiatie rectum (1388), anus (1188) en vulva (1302) te schrappen en daarvoor in de plaats een add-on indicatietekst te maken die tumoragnostisch is:
Capecitabine: bij chemoradiatie als radiosensitizer waarbij er een indicatie is voor 5FU of een 5FU derivaat