
Samenvatting eerder advies
In maart 2021 beoordeelde cieBOM de waarde van durvalumab toegevoegd aan platinumbevattende chemotherapie als eerstelijns palliatieve behandeling bij patiënten met een kleincellig longcarcinoom (SCLC) extensive stage (ES).1 In de fase III-studie CASPIAN werden patiënten met een primair gediagnosticeerd SCLC-ES met meetbare ziekte volgens RECIST 1.1 1:1:1 gerandomiseerd tussen behandeling met durvalumab met chemotherapie, durvalumab en tremelimumab met chemotherapie, of chemotherapie alleen.2 De chemotherapie bestond uit 4 3-wekelijkse cycli etoposide (80-100 mg/m2) op dag 1-3 en carboplatine (AUC 5-6) of cisplatine (75-80 mg/m2) op dag 1. Durvalumab werd in een dosering van 1500 mg intraveneus gegeven, tijdens de chemotherapie 3-wekelijks, vervolgens 4-wekelijks tot aan progressie of onacceptabele toxiciteit. Het primaire eindpunt van de studie was overleving (OS). Behandeling met durvalumab en tremelimumab blijft in dit rapport buiten beschouwing, net als in de eerste beoordeling, omdat er geen EMA-goedkeuring is voor deze combinatie.
Tussen maart 2017 en mei 2018 werden 805 patiënten geïncludeerd door 209 centra in 23 landen: 268 patiënten in de durvalumabgroep en 269 patiënten in de controlegroep. Na een mediane follow-up van 14,2 maanden waren 336 patiënten overleden en vond een geplande interim-analyse plaats. OS was statistisch significant beter in de durvalumabgroep dan in de controlegroep (HR: 0,73 [95%-BI: 0,59-0,91]; p = 0,0047). De mediane OS was 13,0 maanden (95%-BI: 11,5-14,8) in de durvalumabgroep en 10,3 maanden (95%-BI: 9,1-11,2) in de controlegroep.
Bijwerkingen van graad 3-4 traden op bij 62% van de patiënten in beide groepen. De behandeling werd gestaakt ten gevolge van bijwerkingen bij 9% van de patiënten in de beide groepen. Van de patiënten in de durvalumabgroep overleden er 5% aan bijwerkingen en in de controlegroep was dit 6%. De resultaten van het primaire eindpunt OS voldeden niet aan de destijds geldende PASKWIL-criteria voor een positief advies.
Update van de resultaten
In 2022 verschenen de resultaten van de geplande langetermijn-OS-analyse (data-cutoff 22 maart 2021).3 Na mediaan 39,4 maanden waren in de durvalumabgroep nog 44 patiënten (16%) en in de controlegroep nog 13 patiënten (5%) in follow-up. De mediane OS in de durvalumabgroep was 12,9 maanden (95%- BI: 11,3-14,7) en in de controlegroep 10,5 maanden (95%-BI 9,3- 11,2) (HR: 0,71 [95%-BI: 0,60-0,86]). Bij 2 jaar follow-up waren er nog 60 van de 268 patiënten (22,4%) in de durvalumabgroep at risk, waarbij de 2-jaars OS in de durvalumabgroep 22,9% was en in de controlegroep 13,9% (verschil 9,0%). Na 27 maanden waren 54 patiënten (20,1%) in de durvalumabgroep at risk en was nog 20,7% (95%-BI: 16,0-25,7) van de patiënten in de durvalumabgroep in leven en 9,3% (95%-BI: 6,2-13,2) van de patiënten in de controlegroep (11,4% verschil).4 Het voordeel van toevoegen van durvalumab was consistent in de verschillende subgroepen. Wat betreft bijwerkingen lijken er geen grote veranderingen te zijn ten opzichte van de eerder gerapporteerde getallen. Kwaliteit van leven was een secundair eindpunt in de studie en werd bestudeerd met de European Organisation for Research and Treatment of Cancer (EORTC) Quality of Life Questionnaire-Core 30 (QLQ-C30) en de Quality of Life Questionnaire-Lung Cancer 13 (QLQ-LC13). Verschillen tussen baseline en progressie of na 12 maanden follow-up werden voor gespecificeerde klachten (hoesten, kortademigheid, pijn op de borst, moeheid en verlies van eetlust) bestudeerd. Er werd geen verschil gevonden wat betreft verandering van deze klachten tussen beide groepen, behoudens minder verlies van eetlust in de durvalumabgroep. De tijd tot verslechtering van klachten, algemeen functioneren en kwaliteit van leven was langer in de durvalumabgroep dan in de controlegroep.5
In de durvalumabgroep kregen 125 patiënten (46,6%) en in de controlegroep kregen 126 patiënten (46,8%) na progressie een vervolgbehandeling. Deze behandeling bestond uit chemotherapie bij respectievelijk 123 (45,9%) en 119 (44,2%) patiënten, terwijl immuuntherapie bij 6 (2,2%) en 18 (6,7%) patiënten werd gestart.
Bespreking
In de CASPIAN-studie werd een statistisch significant voordeel aangetoond voor het primaire eindpunt OS van eerstelijns palliatieve behandeling met durvalumab toegevoegd aan platinum en etoposide ten opzichte van behandeling met platinum en etoposide bij patiënten met SCLC-ES (HR: 0,73 [95%-BI: 0,59-0,91]; p = 0,0047) met een verschil in de mediane OS van 2,7 maanden. Dit verschil voldeed niet aan de destijds geldende PASKWIL-criteria voor een positief advies.
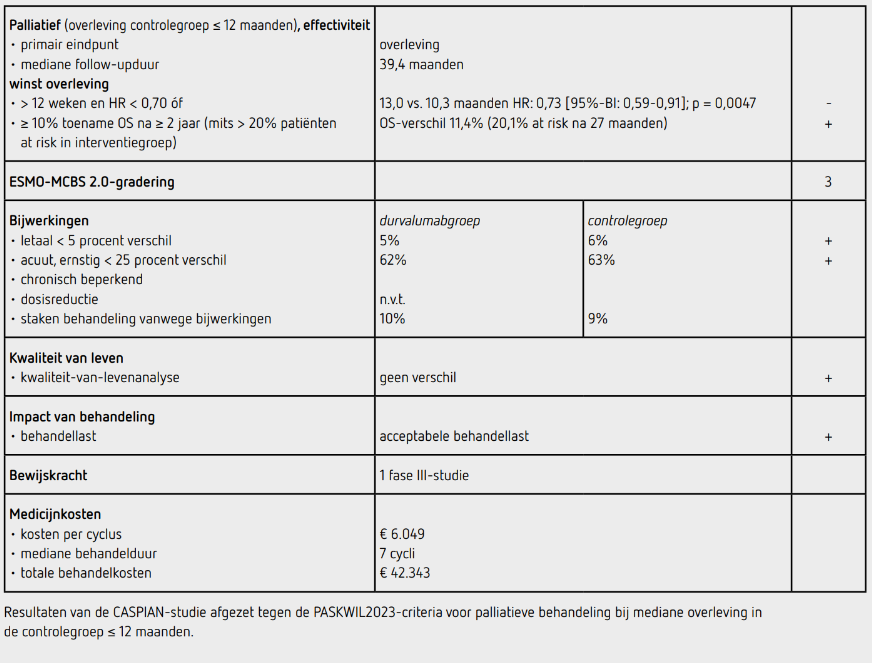
De lange-termijn-OS-analyse van de CASPIAN-studie is inmiddels gerapporteerd. Op basis van de data gegeven in de Kaplan-Meier-curve en beschreven in de tabel van een gepubliceerde subgroepanalyse kan de staart van de OS-curve beoordeeld worden.3,4 In 2024 is het zogenoemde staartcriterium aan de PASKWIL-criteria toegevoegd. Om op basis van het staartcriterium tot een positief advies te komen dient het OS-verschil na ten minste 2 jaar (bij mediane OS in de controlegroep korter dan 12 maanden) ten minste 10% te zijn bij minimaal 20% van de patiënten at risk in de experimentele groep. Na 27 maanden follow-up bedraagt het OS-verschil tussen de behandelgroepen 11,4% terwijl nog 20,1% van de patiënten in de durvalumabgroep at risk is. Op latere tijdpunten in de curve blijft dit verschil bestaan. Op basis hiervan komt cieBOM tot een positief advies volgens de PASKWIL2024-staartcriteria voor palliatieve behandeling waarbij de overleving in de controlegroep korter dan 12 maanden is. De behandeling met durvalumab wordt in het algemeen goed verdragen. Voor SCLC-ES is in augustus 2025 ook serplulimab met chemotherapie voorzien van een positief cieBOM-advies.6
Kosten
De behandeling met durvalumab kost per toediening van 1.500 mg 6.049 euro (bron: medicijnkosten.nl d.d. februari 2026). De kosten van durvalumab (exclusief de kosten van chemotherapie) bij mediaan 7 toedieningen komen daarmee op 42.343 euro.
Conclusie
In de CASPIAN-studie werd een statistisch significant voordeel aangetoond voor het primaire eindpunt OS van eerstelijns palliatieve behandeling met durvalumab toegevoegd aan chemotherapie ten opzichte van chemotherapie alleen bij patiënten met SCLC-ES (HR: 0,73 [95%-BI: 0,59-0,91]; p = 0,0047) met een verschil in de mediane OS van 2,7 maanden. Bij herbeoordeling van de studie op basis van de staartcriteria wordt een OS-verschil van 11,4% gezien tussen de durvalumabgroep en de controlegroep bij een follow-upduur van 27 maanden waarbij 20,1% van de patiënten in de durvalumabgroep at risk is. Deze uitkomsten voldoen aan de PASKWIL2024-staartcriteria voor een positief advies.
Referenties
- NVMO-commissie ter Beoordeling van Oncologische Middelen (BOM). Durvalumab met chemotherapie als eerstelijnsbehandeling voor ‘extensive stage’ kleincellig longcarcinoom. Med Oncol 2021;24(2):27-31.
- Paz-Ares L, Dvorkin M, Chen Y et al. Durvalumab plus platinum-etoposide versus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet 2019; 394(10212):1929-39.
- Paz-Ares L, Chen Y, Reinmuth N et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer: 3-year overall survival update from CASPIAN. ESMO Open 2022;7(2):100408.
- Reinmuth N, Goldman JW, Chen Y et al. Durvalumab plus platinum etoposide in extensive-stage small-cell lung cancer: outcomes in age, sex and platinum subgroups from the phase 3 CASPIAN study. Clin Lung Cancer 2025;26(8):626-41.
- Goldman JW, Garassino MC, Chen Y et al. Patient-reported outcomes with first-line durvalumab plus platinum-etoposide versus platinum-etoposide in extensive-stage small-cell lung cancer (CASPIAN): a randomized, controlled, open-label, phase III study. Lung Cancer 2020; 149:46-52.
- NVMO-commissie ter Beoordeling van Oncologische Middelen (BOM). Serplulimab en chemotherapie bij ‘extensive stage’ kleincellig longcarcinoom. Med Oncol 2025;28(6):28-31.