
Inleiding
De ziekte van Von Hippel-Lindau (VHL) komt bij ongeveer 1 op de 36.000 mensen voor. De aandoening wordt veroorzaakt door een autosomaal dominant overgeërfde mutatie in het VHL-gen op de korte arm van chromosoom 3 met als gevolg accumulatie en activatie van de transcriptiefactor hypoxia-inducible factor 2α (HIF-2α). Patiënten met VHL lopen een levenslang risico op het ontwikkelen van goedaardige en kwaadaardige tumoren of cysten in meerdere organen, waaronder niercelcarcinomen (RCC), hemangioblastomen van de retina of het centrale zenuwstelsel (CZS) en neuro-endocriene tumoren van de pancreas (pNET).1
RCC’s ontstaan bij ongeveer 70% van de patiënten met VHL gedurende hun leven. Er vindt standaard screening van de nieren bij mutatiedragers plaats en indien nodig lokale behandeling met chirurgie, ablatie of radiotherapie. Deze behandelingen moeten vaak herhaald worden en geven toenemende morbiditeit of zijn uiteindelijk niet meer mogelijk zonder verlies van de nierfunctie. CZS-hemangioblastomen komen voor bij tot 80% van de patiënten met VHL. Het zijn vaak sterk gevasculariseerde laesies in de kleine hersenen en het ruggenmerg, maar ook in de hersenstam, cauda equina of de supratentoriële regio. Hoewel ze histologisch als goedaardig worden geclassificeerd, gaan CZS-hemangioblastomen gepaard met aanzienlijke morbiditeit en behoren ze tot de belangrijkste doodsoorzaken bij patiënten met VHL. pNET komt bij 17% van de patiënten met VHL voor. De prognose voor VHL-geassocieerde pNET-tumoren is over het algemeen gunstig omdat deze pNET’s meestal niet-functioneel en asymptomatisch zijn. Belzutifan is een selectieve HIF-2α-remmer die werkzaamheid heeft getoond bij patiënten met VHL- geassocieerde tumoren.
In de hier te bespreken LITESPARK-004-studie wordt de effectiviteit van belzutifan onderzocht bij patiënten met VHL-geassocieerd RCC en andere tumoren.2,3 Belzutifan is door EMA voorwaardelijk geregistreerd voor volwassenen met VHL die behandeling nodig hebben voor een gelokaliseerd RCC, CZS-hemangioblastoom of pNET, en die niet met chirurgie of andere lokale therapieën behandeld kunnen worden.
Kankersoort en lijn van behandeling
Belzutifan werd onderzocht bij patiënten met een VHL-kiembaanmutatie en ten minste 1 niercelcarcinoom kleiner dan 3 cm waarvoor geen chirurgische behandeling nodig was.
Onderbouwing voor een niet-gerandomiseerde studie
VHL is een zeldzaam erfelijk tumorsyndroom en niet alle dragers ontwikkelen een RCC, pNET of CZS-hemangioblastoom. Vanwege de zeer lage incidentie wordt een gerandomiseerde fase II- of III-studie niet haalbaar geacht. Patiënten hebben een levenslang risico en daarbij veelal meerdere soorten tumoren. Belzutifan wordt ingezet als reguliere behandelopties uitgeput zijn. Behandelopties die ingezet kunnen worden, zijn afhankelijk van het tumortype. De biologische rationale voor de werking van de behandeling is sterk en de populatie patiënten is betrouwbaar en reproduceerbaar te selecteren op basis van een kiembaanmutatie in het VHL-gen. Daarmee lijkt beoordeling van een niet-gerandomiseerde studie voldoende onderbouwd.
Methoden van de studie
De LITESPARK-004-studie is een eenarmige fase II-multicenter-studie voor patiënten met een kiembaanmutatie in het VHL-gen en ten minste 1 RCC met een diameter van minimaal 1 en maximaal 3 cm zonder aanwijzingen voor metastasen. Om voor inclusie in aanmerking te komen dienden patiënten 18 jaar of ouder te zijn en een ECOG-performancestatus van 0 of 1 te hebben. Er mocht geen eerdere systeemtherapie gegeven zijn en er mocht geen noodzaak zijn voor een chirurgische behandeling. Patiënten mochten niet behandeld zijn met radiotherapie binnen 4 weken voor inclusie in de studie.
Patiënten kregen belzutifan 120 mg eenmaal daags per os tot aan progressie of onacceptabele bijwerkingen. Dosisreductie in het geval van bijwerkingen was toegestaan. Het primaire eindpunt van de studie was het percentage patiënten met een onafhankelijk vastgestelde en bevestigde objectieve respons (ORR) van de RCC, vastgesteld volgens RECIST 1.1. Secundaire eindpunten waren onder andere tijd tot respons, progressievrije overleving (PFS), duur van de respons (DoR), veiligheid en effectiviteit, waaronder ORR, in VHL-geassocieerde niet-RCC tumoren. Kwaliteit van leven werd niet gemeten.
Bij inclusie in de studie werd een CT- of MRI-scan van de thorax en abdomen verricht en daarnaast een MRI- of CT-scan van de gehele neuro-axis en een oogheelkundig onderzoek. Responsevaluatie middels CT- of MRI-scan, aangevuld met gericht onderzoek bij andere aanwezige VHL-geassocieerde tumoren (bijvoorbeeld MRI-hersenen of fundoscopie) werd elke 12 weken uitgevoerd tot 3 jaar na inclusie en daarna elke 24 weken.
Een objectieve respons moest na ten minste 4 weken middels een nieuwe CT- of MRI-scan bevestigd worden. Bijwerkingen van de behandeling werden geëvalueerd volgens CTC-AE 4.03. Patiënten die stopten met belzutifan werden elke 6 maanden opgevolgd tot de patiënt het consent introk of tot overlijden. Volgens het ontwerp van de studie bestond de geplande omvang van de patiëntengroep uit ongeveer 50 patiënten die ten minste 1 dosis belzutifan hadden gekregen. Uitgaande van een ORR van 30%, werd met deze geplande omvang van de patiëntengroep een 80% power ingeschat om met een eenzijdige alfa van 5% de nulhypothese te verwerpen dat het werkelijke ORR 15% was. De ORR werd separaat berekend voor elk aangedaan orgaansysteem, waarbij per orgaansysteem maximaal 5 targetlaesies en 5 non-targetlaesies werden aangewezen. De finale analyse van het primaire eindpunt werd verricht minimaal 36 weken nadat de laatste patiënt was geïncludeerd.
Effectiviteit van de behandeling afgezet tegen de bijwerkingen
Tussen mei 2018 en maart 2019 werden 61 patiënten in de studie geïncludeerd in 11 centra in de Verenigde Staten, Denemarken, Verenigd Koninkrijk en Frankrijk. De mediane leeftijd van deze patiënten was 41 jaar, 52% was man en 82% had een ECOG-performancestatus van 0. 97% van de patiënten had een eerdere behandeling van de tumor ondergaan zoals partiële nefrectomie, craniotomie of cryoablatie. Bij inclusie in de studie hadden patiënten mediaan 2 RCC’s (bereik 1-5) met een mediane diameter van 22 mm, 22 patiënten (36%) hadden een pNET, 50 patiënten (82%) hadden een CZS-hemangioblastoom en 14 patiënten (23%) hadden een hemangioblastoom van de retina. De mediane follow-up tijdens de meest recente analyse was 49,9 maanden.3 Op het moment van data-cutoff (3 april 2023) gebruikten 36 patiënten (59%) nog belzutifan. De mediane behandelduur was 48,7 maanden.
De ORR in RCC was 67% (95%-BI: 54-79). 7 patiënten (11%) hadden een complete respons en 34 patiënten (56%) hadden een partiële respons. De mediane DoR was nog niet bereikt (95%-BI: 41,3 maanden-niet bereikt). De mediane PFS was 49,8 maanden (95%-BI: 49,8-niet bereikt). Bij 20 van de 22 evalueerbare patiënten met een VHL-geassocieerde pNET werd een radiologische respons vastgesteld (ORR 91% [95%-BI: 71-99]), waarvan bij 11 patiënten (50%) sprake was van een complete respons. De mediane DoR was nog niet bereikt (95%-BI: niet bereikt-niet bereikt). Bij 24 van de 50 patiënten met CZS-hemangioblastoom werd een respons vastgesteld, waarvan bij 4 patiënten (8%) sprake was van een complete respons. De ORR was 48% (95%-BI: 34-63) waarbij de mediane DoR niet bereikt was (95%-BI: niet bereikt-niet bereikt).
Behandelingsgerelateerde bijwerkingen van graad 3 kwamen voor bij 11 patiënten (18%). De meest frequent voorkomende behandelingsgerelateerde bijwerking van graad 3 was anemie en kwam voor bij 7 patiënten (11%). Behandelingsgerelateerde bijwerkingen van graad 4 of 5 werden niet vastgesteld. Tijdens de behandeling zijn 2 patiënten overleden, maar bij geen van deze overlijdens werd een relatie met de behandeling verondersteld. Vanwege behandelingsgerelateerde bijwerkingen werd de behandeling onderbroken bij 13 patiënten (21%) en bij 10 patiënten (16%) werd de dosis gereduceerd. Bij 2 patiënten (3%) werd de behandeling gestaakt vanwege bijwerkingen.
Kwaliteit van de studie en interpretatie van de uitkomsten
Zonder vergelijkende arm en met beperkte aantallen patiënten is de kwaliteit van deze studie matig. Er is wel een sterke biologische rationale en een redelijke follow-upduur. De studie is uitgevoerd in oncologische expertisecentra. De data komen consistent over. Het aantal geïncludeerde patiënten was hoger dan het beoogde aantal. Hierdoor kan het 95%-betrouwbaarheidsinterval smaller zijn dan van tevoren ingeschat. Er vond geen formele hypothesetoetsing plaats. Er vond ook geen correctie voor multipele testen plaats. Ook zijn in het statistisch plan van de studie geen grenzen voor effectiviteit omschreven voor de niet-RCC VHL-geassocieerde tumoren. De ORR werd volgens RECIST 1.1 per orgaansysteem vastgesteld en niet per patiënt, waardoor een patiënt een separate responsevaluatie voor RCC en voor elke andere VHL-geassocieerde tumor kreeg.
Discussie
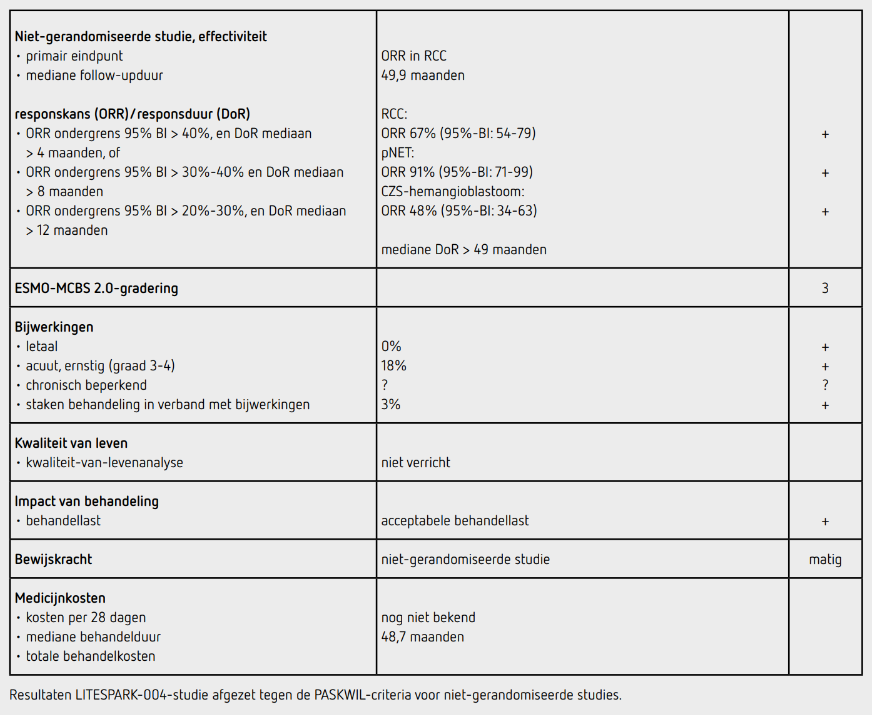
Belzutifan geeft bij patiënten met VHL-geassocieerd RCC, pNET en CZS hemangioblastoom een ORR van respectievelijk 67% (95%-BI: 54-79), 91% (95%-BI: 71-99) en 48% (95%-BI: 34-63), waarbij de mediane DoR niet bereikt is bij een mediane follow-up van meer dan 4 jaar. Deze resultaten voldoen aan de PASKWIL-criteria voor niet-gerandomiseerde studies voor een voorlopig positief advies. Het advies is voorlopig vanwege de voorwaardelijke goedkeuring door EMA.
Opvallend is dat EMA belzutifan heeft goedgekeurd voor patiënten die behandeling nodig hebben voor hun VHL-geassocieerde tumor, terwijl dit voor de patiënten die participeerden in de LITESPARK-004-studie niet het geval was. Het is daardoor niet duidelijk of de resultaten van de studie direct te extrapoleren zijn naar de groep patiënten waarvoor deze behandeling geregistreerd is. Bij langere follow-up neemt de ORR nog steeds toe. Dat betekent dat het niet eenvoudig is om een maximale behandelduur aan te geven. Dit zou in de praktijk problemen kunnen opleveren omdat het vaak indolente tumoren betreft die op jonge leeftijd voorkomen en een gunstige prognose kennen. Zowel vanuit patiëntperspectief als vanuit maatschappelijk perspectief lijkt langdurige of zelfs levenslange behandeling met belzutifan onwenselijk. De bijwerkingen zijn over het algemeen beheersbaar. Belzutifan is ook onderzocht bij patiënten met een niet-VHL-geassocieerd RCC in een gerandomiseerde studie waarbij patiënten in de controlegroep everolimus kregen.4 Deze indicatie is hier buiten beschouwing gelaten.
Kosten
De kosten van belzutifan in Nederland zijn nog niet bekend (bron: medicijnkosten.nl, dd. maart 2026).
Conclusie
Bij patiënten met VHL-geassocieerd RCC, pNET en CZS hemangioblastoom resulteert behandeling met belzutifan in een ORR van respectievelijk 67% (95%-BI: 54-79), 91% (95%-BI: 71-99) en 48% (95%-BI: 34-63), waarbij bij een mediane follow-up van meer dan 4 jaar de mediane DoR niet bereikt is. Deze uitkomsten voldoen aan de PASKWIL-criteria voor niet-gerandomiseerde studies voor een voorlopig positief advies. Dit advies is tot stand gekomen op basis van de uitkomsten van niet-gerandomiseerde onderzoek. De kwaliteit van het bewijs is matig. Het is waarschijnlijk dat met verder onderzoek de schatting van de grootte van het effect van de behandeling zal veranderen.
Referenties
- Lonser RR, Glenn GM, McClellan W et al. Von Hippel-Lindau disease. Lancet 2003;361(9374):2059-67.
- Jonasch E, Donskov F, Iliopoulos O et al. Belzutifan for renal cell carcinoma in von Hippel-Lindau disease. N Engl J Med 2021;385(22):2036-46.
- Srinivasan R, Iliopoulos O, Beckermann KE et al. Belzutifan for von Hippel-Lindau disease-associated renal cell carcinoma and other neoplasms (LITESPARK-004): 50 months follow-up from a single-arm, phase 2 study. Lancet Oncol 2025;26(5):571- 82.
- Choueiri TK, Powles T, Peltola K et al. LITESPARK-005 Investigators. Belzutifan versus Everolimus for Advanced Renal-Cell Carcinoma. N Engl J Med 2024;391(8):710-21.