
In Nederland zijn momenteel olaparib (SOLO-1-studie) en niraparib (PRIMA-studie) beschikbaar als onderhoudsbehandeling bij een primair stadium III-IV hooggradig epitheliaal ovariumcarcinoom na een initiële respons op platinumbevattende chemotherapie.
Olaparib is beschikbaar voor patiënten met een kiembaan- of somatische BRCA-mutatie. Niraparib was ook beschikbaar voor patiënten met een ovariumcarcinoom met homologe-recombinatiedeficiëntie (HRD). Het eerdere voorlopig positieve advies van niraparib komt echter te vervallen op basis van de recente OS-data waar geen overlevingsvoordeel werd aangetoond. Voor rucaparib, de derde PARP-remmer, is er momenteel een voorlopig positief commissie BOM-advies op basis van de ATHENA-MONO-studie. Dit betreft onderhoudsbehandeling na primaire therapie van patiënten met een tumor met een (germline of somatische) BRCA-mutatie, maar ook patiënten met HRD en patiënten met homologe-recombinatieproficiënte (HRP) tumoren.
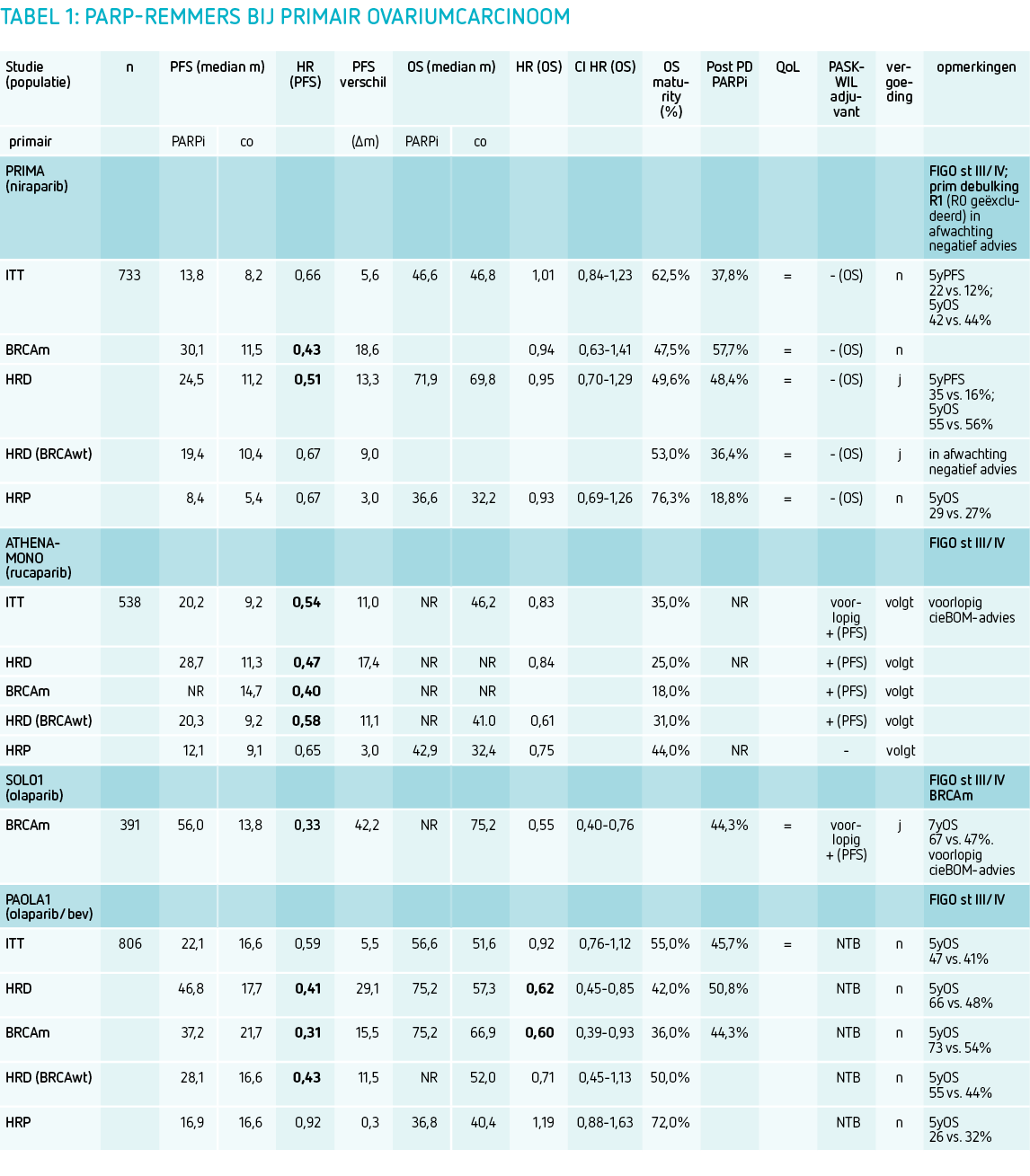
De verrichte eerstelijn studies met PARP-remmers verschillen onderling in studiedesign, onderhoudsbehandeling met verschillende PARP-remmers, al of niet gecombineerd met bevacizumab, duur van de behandeling, patiëntenselectie t.a.v. chirurgische resultaten en tumorkenmerken met betrekking tot BRCA- en HRD-status en populatie van primaire analyse. Hierdoor is een onderlinge vergelijking maar beperkt mogelijk. In alle studies was PFS het primaire eindpunt. Hieronder worden de belangrijkste uitkomsten van de studies in de primaire setting benoemd (tabel 1).
Uitkomsten van studies in primaire setting
In de SOLO1-studie gaf 2 jaar onderhoudsbehandeling met olaparib bij vrouwen met een FIGO-stadium III-IV primair ovariumcarcinoom, hooggradig sereus (HGS) en endometroïd type en een BRCA1/2-mutatie bij een complete of partiële respons na chemotherapie (indien van toepassing) een significant mediaan PFS-voordeel van 42,2 maanden (mediane PFS: 56,0 vs. 13,8 mnd, HR: 0,33). Na 7 jaar follow up was 67,0 procent van de vrouwen met olaparib ten opzichte van 46,5 procent met placebo in leven (HR OS: 0,55, bij deze analyse nog net niet statistisch significant verschillend aangetoond). Dit overlevingsverschil werd bereikt ondanks postprogressiebehandeling met een PARP-remmer bij 44,3 procent van de vrouwen in de controlegroep.1
In de PRIMA-studie werden 733 vrouwen geïncludeerd met een primair ovariumcarcinoom, FIGO-stadium III-IV, voornamelijk met een hooggradig sereus of endometroïd subtype, na complete of partiële respons op behandeling. Patiënten met stadium III ziekte met een complete primaire debulking werden geëxcludeerd. Geïncludeerde patiënten kregen maximaal 3 jaar onderhoudsbehandeling met niraparib of placebo, hetgeen leidde tot een verbetering in mediane PFS in de ITT-populatie.
De winst in PFS was zoals verwacht het grootst in de BRCA1/2-gemuteerde groep (30,1 versus 11,5 mnd, HR: 0,43), in de HRD-groep (24,5 versus 11,2 mnd, HR: 0,51) en in de HRD-groep zonder BRCA-mutatie (19,4 versus 10,4 mnd, HR: 0,67), wat klinisch relevante verschillen zijn. In de HRP-groep was de PFS-winst klinisch niet relevant. Recent werden de OS-resultaten gepubliceerd die voor geen enkele subgroep OS-winst lieten zien.2 Hiermee komt het voorlopige positieve commissie BOM-advies te vervallen. De overlevingsuitkomsten waren wel opvallend gunstig met een mediane overleving van 48,8 maanden en een 5-jaars OS van 42 procent in de ITT-populatie en van 55 procent in de HRD-populatie. Na ziekteprogressie kreeg 48,4 procent in de HRD-populatie alsnog behandeling met een PARP-remmer, wat van invloed is geweest op de OS-resultaten.
In de ATHENA-MONO-studie werden 538 vrouwen geïncludeerd met een primair ovariumcarcinoom, FIGO-stadium III-IV, met een randomisatie tussen onderhoudsbehandeling met rucaparib of placebo, waarbij de PFS in de HRD-populatie en in de totale populatie het primair eindpunt waren. De mediane PFS was 28,7 versus 11,3 maanden (HR: 0,47) in de HRD-populatie. In de ITT-populatie was de PFS 20,2 versus 9,2 maanden (HR: 0,52) en in de HRP-populatie was de PFS 12,1 versus 9,1 maanden (HR: 0,65). OS-data zijn nog niet matuur. Deze uitkomsten voldoen aan de PASKWIL-criteria voor een voorlopig positief advies voor alle geïncludeerde patiëntengroepen.
Naast de drie studies die door cieBOM zijn beoordeeld is ook de PAOLA-1-studie in deze setting uitgevoerd. In deze studie kregen patiënten systeemtherapie bestaande uit paclitaxel, carboplatine en bevacizumab. In deze studie kregen 806 vrouwen met primair ovariumcarcinoom, FIGO-stadium III-IV, na respons op chirurgie en chemotherapie, 2 jaar onderhoudsbehandeling met olaparib of placebo. Bevacizumab werd tot maximaal 15 maanden gecontinueerd.
Omdat langetermijndata van enkele studies nog volgen, is de optimale plaats van de behandeling nog niet duidelijk
Onderhoudsbehandeling met de PARP-remmer in combinatie met bevacizumab (EMA-registratie) leidde tot ongeveer 5,5 maanden verschil in PFS in de ITT-populatie ten faveure van olaparib en bevacizumab. De PFS-winst werd gevonden in de patiënten met een BRCA1/2-gemuteerde tumor of een HRD-tumor. Gepubliceerde OS-data lieten ook een significante OS-winst zien voor olaparib in deze populaties (BRCAm 75,2 versus 66,9 maanden, HR: 0,60 en HRD: 75,2 versus 57,3 maanden, HR: 0,62).10,11 De PAOLA-1-studie is niet beoordeeld door cieBOM, omdat in Nederland bevacizumab niet standaard wordt gegeven bij de primaire behandeling van het ovariumcarcinoom.
Juiste patiënten identificeren
In geen van de studies was de kwaliteit van leven significant verschillend ten opzichte van de standaardbehandeling, ondanks de bijwerkingen die veelvuldig voorkomen bij PARP-remmers. Bij een lange behandelduur blijkt 98 procent bijwerkingen te krijgen, waaronder bijwerkingen graad 3 (meestal hematologisch), wat in 28 procent leidt tot dosisreductie en in 50 procent tot dosisinterruptie. In de praktijk gebeurt dit veelal in de eerste weken van de behandeling, waarna de behandeling goed verdragen wordt.
De belangrijkste vragen voor de klinische praktijk zijn hoe men de juiste patiënten kan identificeren die baat zullen hebben bij een PARP-remmer. Een factor die meegenomen moet worden is de effectgrootte van de winst in de diverse subgroepen op basis van de aanwezigheid van een BRCA-mutatie en HRD of HRP. De grootste winst wordt bereikt in de patiëntenpopulatie met een BRCA1/2-mutatie, gevolgd door de HRD/BRCAwt-populatie. In de HRP/BRCAwt-populatie is de PFS-winst klinisch weinig relevant (PRIMA-studie, ATHENA-MONO-studie) of afwezig (PAOLA-1-studie). De studies hebben niet dezelfde testen gebruikt om homologe recombinatie vast te stellen (myChoice CDx, Myriad of FoundationOne CDx, Foundation Medicine Inc), waarbij er nog geen eenduidige test is voor het bepalen van de HRD-status.
Optimale standaardbehandeling
Nu er meer langetermijnresultaten beschikbaar zijn van de studies bij de behandeling van het primair en gerecidiveerd ovariumcarcinoom rijst de vraag wat de optimale standaardbehandeling van het stadium III/ IV primair ovariumcarcinoom is en wanneer een PARP-remmer het beste kan worden ingezet. Voor de vrouwen met een BRCA-gemuteerd ovariumcarcinoom gaat de sterke voorkeur uit naar behandeling in de primaire setting, omdat er in deze setting een (waarschijnlijke) OS-winst wordt verwacht met PARP-remmers (olaparib). De absolute PFS-winst is in de primaire behandeling bij patiënten met een BRCA-mutatie ook beduidend groter dan bij het recidief. Bovendien is de behandelduur waarschijnlijk korter, namelijk 2 jaar versus tot aan progressie.
Voor de vrouwen zonder een BRCA-mutatie maar met een HRD laten de meeste studies tot nu toe wel een grote PFS-winst maar geen OS-winst zien. Langetermijndata van enkele studies volgen nog (ATHENA-MONO, PRIME, FIRST). Daarom geldt dan ook dat de optimale plaats van de behandeling nog niet helemaal duidelijk is.
Meer onderzoek is nodig om te bepalen of een PARP-remmer beter als onderhoudsbehandeling na primaire behandeling of na platinumbevattende chemotherapie voor een recidief ovariumcarcinoom gegeven kan worden. Voorwaarde voor behandeling in welke setting dan ook, is patiëntenselectie door middel van een optimale en betrouwbare HRD-test.
SAMENVATTING
De huidige indicaties voor een PARP-remmer bij het ovariumcarcinoom worden:
- Patiënten met een stadium III/IV hooggradig sereus of endometroïd ovariumcarcinoom, met een kiembaan- of somatische BRCA-mutatie, met een partiële of complete respons op primaire behandeling met platinumbevattende chemotherapie komen in aanmerking voor 2 jaar olaparib.
- Patiënten met een stadium III/IV hooggradig sereus of endometroïd ovariumcarcinoom (zonder BRCA-mutatie), na primaire of intervaldebulking en minstens partiële respons op chemotherapie kunnen als de vergoedingsstatus bekend is behandeld worden met 2 jaar rucaparib. Het klinisch voordeel is het grootst bij HRD-tumoren. Of patiënten met een HRP-tumor baat hebben van behandeling is niet uit de ATHENA-MONO-studie af te leiden. Omdat uit andere studies bekend is dat patiënten met een HRP-tumor nauwelijks baat hebben van behandeling met een PARP-remmer en het vaak tot bijwerkingen leidt, is ons advies om de HRP-populatie hier niet mee te behandelen.
- Patiënten met een platinumsensitief recidief ovariumcarcinoom, na minstens partiële respons op chemotherapie, ongeacht BRCA-status, komen in aanmerking voor olaparib, respectievelijk niraparib, tot aan progressie.
Referenties
- Mirza MR, Monk BJ, Herrstedt J, et al. Niraparib maintenance therapy in platinum-sensitive, recurrent ovarian cancer. N Engl J Med 2016;375(22):2154-64.
- Ledermann JA, Harter P, Gourley C, et al. Overall survival in patients with platinum-sensitive recurrent serous ovarian cancer receiving olaparib maintenance monotherapy: an updated analysis from a randomised, placebo-controlled, double-blind, phase 2 trial. Lancet Oncol 2016;17(11):1579-89.
- Moore K, Colombo N, Scambia G, et al. Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med 2018;379(26):2495-505.
- Banerjee S, Moore KN, Colombo N, et al. Maintenance olaparib for patients with newly diagnosed advanced ovarian cancer and a BRCA mutation (SOLO1/GOG 3004): 5-year follow-up of a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2021;22 (12):1721-31.
- DiSilvestro P, Banerjee S, Colombo N, et al. Overall survival with maintenance olaparib at a 7-year follow-up in patients with newly diagnosed advanced ovarian cancer and a BRCA mutation: The SOLO1/GOG 3004 Trial. J Clin Oncol. 2022;41(3):609-17.
- Ray-Coquard I, Pautier P, Pignata S et al. Olaparib plus bevacizumab as first-line maintenance in ovarian cancer. N. Engl. J. Med 2019;381(25);2416-28.
- Ray-Coquard I, Leary A, Pignata S, et al. Olaparib plus bevacizumab first-line maintenance in ovarian cancer: final overall survival results from the PAOLA-1/ENGOT-ov25 trial. Ann Oncol 2023;34(8):681-92
- González-Martín, A. et al. Niraparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med 2019;381(25):2391-402.
- Li N, Zhu J, Yin R, et al. Treatment with niraparib maintenance therapy in patients with newly diagnosed advanced ovarian cancer a phase 3 randomized clinical trial. JAMA Oncol 2023;9(9):1230-3.
- Monk BJ, Parkinson C, Lim MC, et al. A randomized, phase iii trial to evaluate rucaparib monotherapy as maintenance treatment in patients with newly diagnosed ovarian cancer (ATHENA-MONO/GOG-3020/ENGOT-ov45). J Clin Oncol 2022;40(34):3952-64.
- Monk BJ, Barretina-Ginesta MP, Pothuri B, et al. Niraparib first-line maintenance therapy in patients with newly diagnosed advanced ovarian cancer: final overall survival results from the PRIMA/ENGOT-OV26/GOG-3012 trial. Ann Oncol 2024;35(11):981-92.