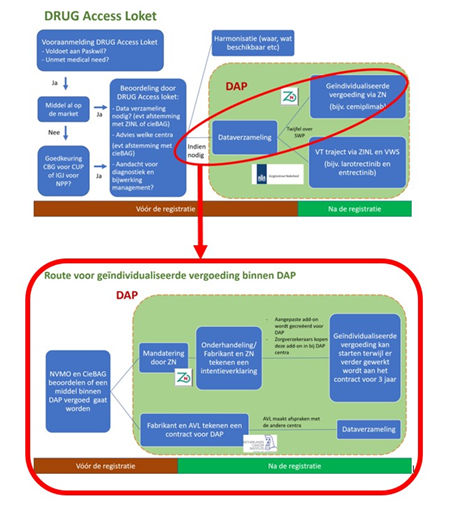
Drug Access Protocol (DAP) streeft naar het sneller, gecontroleerd en gecoördineerd beschikbaar stellen van veelbelovende medicatie die nog niet in het basispakket zit. Aan de hand van metingen en observaties worden gegevens over de effectiviteit en bijwerkingen van de medicatie verzameld. Hierdoor is het beter mogelijk om sneller te bekijken of middelen in aanmerking komen voor opname in het basispakket.
Breed gedragen initiatief
DAP is een initiatief van de Nederlandse Vereniging voor Medische Oncologie (NVMO), de Nederlandse Vereniging van Artsen voor Longziekten en Tuberculose (NVALT), het Antoni van Leeuwenhoek, Zorginstituut Nederland (ZiNL) en Zorgverzekeraars Nederland (ZN).
Toegang en betaling
Voordat geneesmiddelen mogen worden voorgeschreven, moet eerst zijn bewezen dat ze effectief en veilig zijn. Voor geneesmiddelen tegen minder vaak voorkomende vormen van kanker zijn er vaak zo weinig patiënten, dat het lang duurt voordat voldoende gegevens zijn verzameld om daarover uitspraken te kunnen doen. De kleine klinische studies waarop de markttoelating van veelbelovende middelen gebaseerd zijn, kunnen niet alle vragen met betrekking tot de doeltreffendheid van een behandeling beantwoorden. Met dit protocol wordt de toegang en betaling geregeld, terwijl aanvullende data over effect en bijwerkingen verzameld wordt.
Gestructureerd gegevens verzamelen
Veel sneller dan via de tot nu toe gebruikelijke procedure komt veelbelovende medicatie hierdoor al gecontroleerd beschikbaar voor patiënten. DAP helpt internist-oncologen en longartsen enorm bij de toegang tot een nieuwe behandeling en het gestructureerd verzamelen van gegevens over deze behandeling.
Versnelling beschikbaarheid in Nederland
Streven is om uiteindelijk alle named patient- en compassionate use-programma’s, waarbij het draait om veelbelovende, maar niet in Nederland in het basispakket vergoede medicatie, onder DAP te laten vallen. Dit geldt ook voor veelbelovende nieuwe medicatie. Op dit moment is er soms een lange wachttijd voor het beschikbaar komen van medicatie voor patiënten met meer zeldzame tumoren waar nog onvoldoende goede studies voor zijn. Door gebrek aan data is het moeilijk te beoordelen wat de middelen voor de patiënt doen en of ze voor opname in het basispakket in aanmerking komen. DAP zet in op versnelling van dit proces.
Criteria voor beoordeling door DAP
Onderstaande voorwaarden voor oncologische middelen zijn van toepassing om in aanmerking te komen voor toelating tot DAP.
- Een zeldzame indicatie én
- Unmet medical need naar beoordeling van de commissie én
- Een positieve CHMP-mening of formele EMA-registratie voor de betreffende indicatie óf
- Een FDA-registratie én geïnitieerd registratieproces bij de EMA én
- Gepubliceerde resultaten in een peer reviewed medisch tijdschrift
Protocol
Raadpleeg voor verdere informatie over governance, aanmeldprocedure, benodigde documenten en vervolgstappen onderstaand protocol.
![]() Protocol DAP
Protocol DAP
Commissie DAP
De commissie DAP wordt gevormd door internist-oncologen prof. dr. Haiko Bloemendal (voorzitter), dr. Ferry Eskens en prof. dr. An Reyners, en longarts prof. dr. Egbert Smit (namens NVALT).
Meer informatie
Bij vragen over DAP kan worden gemaild naar drugaccess@nvmo.org.